影响水的pH值的因素
有许多因素会影响水中的pH值,无论是天然的还是人造的。大多数自然变化是由于与周围岩石(尤其是碳酸盐形式)和其他物质的相互作用而发生的。pH值也会随降水(尤其是酸雨)和废水或采矿废水的排放而波动13。此外,CO2浓度会影响pH值。
二氧化碳和pH
二氧化碳是水中酸的zui常见原因。由于光合作用,呼吸作用和分解作用对CO2水平的影响,它们均会导致pH波动。这些变化的极端程度取决于水的碱度,但通常会有明显的昼夜(每天)变化¹。在呼吸和分解率很高的水域中,这种影响更容易测量。
二氧化碳以溶解状态(如氧气)存在于水中,但它也可以与水反应生成碳酸:
CO2 + H2O <=> H2CO3
然后,H2CO3会失去一个或两个氢离子:
H2CO3 <=> HCO3 – + H +…。HCO3 – <=> CO3 2- + H +
释放的氢离子使水的pH降低。但是,该方程式可以根据当前的pH值在两个方向上运行,并作为其自身的缓冲系统。在较高的pH值下,该碳酸氢盐系统将向左移动,而CO3 2-将吸收自由的氢离子。
由于H2CO3的溶解常数低(亨利定律),该反应通常很少。但是,随着世界范围内CO2含量的增加,溶解的CO2量也增加,该方程式将从左向右执行。这会增加H2CO3,从而降低pH。随着时间的推移,这种影响在海洋pH研究中变得越来越明显。
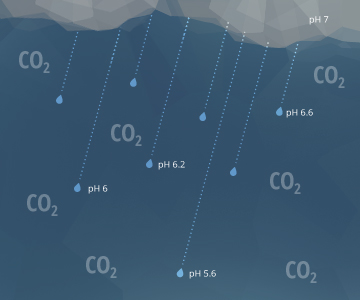
上面的等式也解释了为什么雨水的pH值约为5.65 -1。当雨滴从空中掉落时,它们与大气中的二氧化碳分子相互作用。这会在雨滴中产生H2CO3,使雨水的pH值降低¹⁷。pH值为5.65,尽管是酸性的,却不认为是酸雨。假定标准大气中的二氧化碳浓度为0.0355%-1,则自然,无污染的雨或雪的pH值预计将接近5.6。酸雨要求pH值低于5.0²¹。
5.65也是与空气平衡且未与碳酸盐材料或石灰石接触的水的pH值。
天然pH值的影响
碳酸盐材料和石灰石是可以缓冲水中pH值变化的两个元素。碳酸钙(CaCO3)和其他碳酸氢盐可与氢或氢氧根离子结合以中和pH值。当土壤中存在碳酸盐矿物时,水的缓冲能力(碱度)会增加,即使添加酸或碱,水的pH值也接近中性。除此之外的其他碳酸盐材料可使中性水略带碱性。

如前所述,未污染的雨水呈弱酸性(pH值为5.6)。雨水的pH值也可能由于火山灰,湿地中减少硫酸盐的细菌,野火引起的空气传播颗粒甚至闪电¹而降低。如果雨水落在缓冲性差的水源上,则会通过径流降低附近水的pH值。
松针或冷杉针还可以分解土壤,从而降低土壤以及流经土壤的水的pH值。强烈的光合作用会去除水中的二氧化碳,从而增加水的pH值,尽管这种变化通常是昼夜的。
人造pH影响者
pH波动的人为原因通常与污染有关。酸雨是人类对水pH值影响的zui著名例子之一。pH值小于5.0的任何形式的沉淀都称为酸雨²。这种沉淀来自水与氮氧化物,硫氧化物和其他酸性化合物的反应,从而降低了已经微酸性的pH值。这些排放物通常来自采矿和冶炼作业或化石燃料燃烧(燃煤和汽车)¹⁸。极高的二氧化碳含量还可以进一步降低雨水的pH值。
点源污染是常见的原因,可以根据所涉及的化学物质增加或降低pH值。这些化学物质可能来自农业径流,废水排放或工业径流。如果周围土壤缓冲不良,则采矿作业(特别是煤炭)会产生酸性径流和酸性地下水渗流。包含清洁剂和肥皂基产品的废水排放会导致水源变得太碱性。