海洋酸化
海洋酸化是由溶解的二氧化碳大量涌入引起的。由于人为原因导致大气中的CO2含量增加时,溶解的CO2含量也增加,从而降低了水的pH值。
当水被二氧化碳饱和时,它不仅会降低海洋的pH值,还会消耗碳酸钙源和³3。碳酸钙CaCO3是建造许多水生生物的珊瑚,贝壳和外骨骼的必要成分。随着CO3²水平的降低,海洋生物建造贝壳的难度变得更大。
如“二氧化碳和pH值”部分所述,额外的CO2会增加水中的氢离子数量,从而降低pH值:
CO2 + H2O <=> H2CO3…H2CO3 <=>(H +)+HCO3⁻
在pH值介于6.4和10.33之间的情况下,其中一些氢离子会附着在碳酸根离子上²²:
(H +)+ CO3 2- <=> HCO3 –
因此,随着CO2含量的增加,碳酸盐,CO3 2-的可用性降低,从而减少了贝壳和珊瑚建筑物的可利用量。
CO2 + H2O +CO3²⁻<=>2HCO3⁻
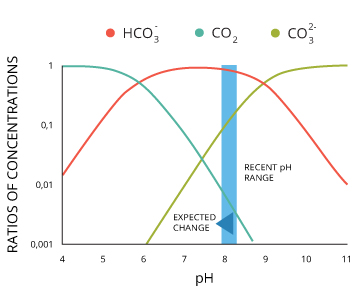
高的二氧化碳含量也由于较低的pH值和与碳酸盐的竞争而使维持当前的外壳更加困难。
此外,水的空气饱和度基于亨利定律的分压。随着空气中二氧化碳含量的增加,其分压也随之增加。这样可以降低氧气的分压,降低其饱和度,并导致低氧(低O2)条件。
虽然海洋永远不会变成“酸性”(pH值小于7),但即使pH值降低一点点,也会给咸水生物带来压力并增加死亡率。pH是对数的,意味着降低0.1相当于酸度增加了30%。